Plötzlicher Herztod
Plötzlicher Herztod (PHT) oder Sekundentod ist ein medizinischer Fachausdruck für einen plötzlich und unerwartet eingetretenen Tod kardialer Ursache. Im angloamerikanischen Sprachraum ist die Bezeichnung Sudden Cardiac Death (SCD) gebräuchlich.
Der unwiderrufliche Tod ist hierbei meist Folge eines anhaltenden Kammerflimmerns oder einer anhaltenden Kammertachykardie, die dann zum Herzstillstand führen. Wird einer dieser Zustände durch Defibrillation / Cardioreversion oder manuelle Wiederbelebungsmaßnahmen erfolgreich und dauerhaft beendet, wird die Formulierung überlebter plötzlicher Herztod oder Zustand nach Reanimation verwendet.
Häufigkeit
Der plötzliche Herztod stellt die häufigste tödliche Manifestationsform einer Herzerkrankung dar. In Deutschland versterben an ihr ca. 130.000 bis 200.000 Menschen pro Jahr. Rund 40% dieser Menschen könnten noch leben,wenn frühzeitig ein Defibrillator eingesetzt worden wäre. Dieser Anteil ist trotz Senkung der allgemeinen kardiovaskulären Mortalität konstant. Bei dem Vorliegen einer klinisch relevanten Herzerkrankung ist das Risiko, einen PHT zu erleiden, 6- bis 10-fach erhöht; allein eine Koronare Herzerkrankung erhöht das Risiko um das 2- bis 4-fache. Männer sterben häufiger den plötzlichen Herztod als Frauen (Männer/Frauen pro 100.000: 410,6/274,6), die Mortalität steigt mit dem Alter (Männer/Frauen pro 100.000: 35-44 Jahre 34,1/11,5; 75-84 Jahre 1362,8/928,5)[1]. Im Weiteren ist das Risiko, einen plötzlichen Herztod beim Sport zu erleiden, für Leistungssportler 2,5 mal so hoch wie für Nicht-Sportler[2].
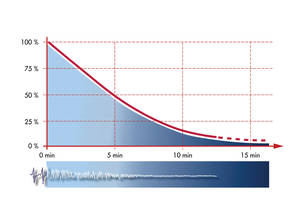
Die Überlebensrate fällt in jeder Minute um 10% wenn keine Hilfe zuteil wird.
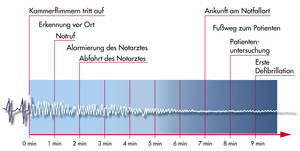
Die Hilfszeiten betragen zwischen 4-9 Minuten bis adequate Hilfe erscheint wie DRK Ersthelfer , Rettungdienst oder Notarzt. Siehe Graphik.
Ursachen
Für das Auftreten eines PHT braucht es in der Regel drei Komponenten:
- Strukturelle Herzerkrankung
- Vorübergehender Auslöser
- Arrhythmie-Mechanismus
Es kommt zu einer Herzrhythmusstörung, einer elektromechanischen Entkoppelung oder auch sofort zu einer Asystolie. Am Beginn einer Rhythmusstörung steht häufig eine Ventrikuläre Tachykardie, die sich dann in Kammerflimmern wandelt. Es folgt dann hypoxiebedingt die Asystolie ohne elektrische Aktivität am Herzen. Seltener kann sich auch aus einer Bradykardie, z. B. im Rahmen eines AV-Block III° oder Bradyarrhythmie, eine Asystolie entwickeln.
Strukturelle Herzerkrankung
Koronare Herzkrankheit (ca. 80 % der Fälle)
- Bei 15-50% der Patienten (Zahlen variieren stark in Abhängigkeit von der Literatur) handelt es sich um die Erstmanifestation einer Koronaren Herzerkrankung (KHK).[3]
- Akuter Herzinfarkt: Innerhalb der ersten 48 Stunden nach einem unbehandelten Herzinfarkt besteht eine 15-prozentige Wahrscheinlichkeit, einen plötzlichen Herztod (PHT) zu erleiden. Dieses Risiko fällt in den nächsten Tagen auf 3 % ab. 80 % aller Episoden von Kammerflimmern ereignen sich in den ersten sechs Stunden nach Schmerzbeginn (Maximum in der ersten Stunde) bei akutem Herzinfarkt.
- Chronische KHK: 50 % der Patienten hatten bereits einen Myokardinfarkt. Hier spielen ventrikuläre Tachykardien aus den Narbengebieten eine wesentliche Rolle.
Nichtischämische Kardiomyopathien (ca. 10-15 % der Fälle)
Hierunter versteht man Herzmuskelerkrankungen die nicht durch eine koronarer Herzerkrankung, z.B. im Rahmen eines Herzinfarktes entstanden sind. Es zählen hierzu:
- Dilatative Kardiomyopathie (DCM): 30 % aller Todesfälle bei Patienten mit DCM treten plötzlich auf.
- Hypertrophe Kardiomyopathie (HCM): Besondere Risikofaktoren sind u. a. eine stark verdickte Wand des linken Herzens und ein unzureichender Blutdruckanstieg bei Belastung. Die HCM ist die häufigste Ursache des plötzlichen Herztodes bei jungen Menschen.
Seltene Ursachen (<5 %)
- Arrhythmogene rechtsventrikuläre Kardiomyopathie (ARVCM): Risiko besonders erhöht bei eingeschränkter rechtsventrikulärer Pumpfunktion.
- Long-QT-Syndrom: Synkopen sind die häufigste Manifestation. Je jünger der Patient beim Auftreten der ersten Synkope, desto schlechter ist die Prognose. 20% sterben innerhalb eines Jahres nach der ersten Synkope
- Brugada-Syndrom: Der PHT wird durch schnelle polymorphe Kammertachykardien vorzugsweise in Ruhephasen oder im Schlaf verursacht.
- Idiopathisches Kammerflimmern: Das ist eine sogenannte Ausschlussdiagnose, die bei ca. 8 % der Überlebenden eines plötzlichen Herzstillstandes mit strukturell gesundem Herzen gestellt wird.
- Aortenstenose (AS): Vor der Zeit der Aortenklappenchirurgie war die AS eine häufige nichtkoronare Ursache des plötzlichen Herztodes. 73 % der Patienten mit hochgradiger AS starben hieran. Nach Aortenklappenersatz sind 18 bis 21 % aller Todesfälle plötzliche Herztode (Häufigkeitsgipfel 3 Wochen bis 8 Monate nach Operation).
Weitere seltene Ursachen
- Koronaranomalien, Koronararterienembolien, Koronararteriitis, Koronarspasmen und Muskelbrücken
- peripartale Kardiomyopathie (Mortalität innerhalb der Schwangerschaft 20%)
- Entzündliche und infiltrative Erkrankungen des Herzens (Myokarditis, Autoimmunerkrankungen, Amyloidose, Hämochromatose, Chagas-Kardiomyopathie
- neuromuskulären Erkrankungen.
Vorübergehende Auslöser
- Elektrolytstörungen (Veränderungen der Blutsalze):
- Hypokaliämie <2,5 mmol/l, Hyperkaliämie > 6,5 mmol/l[4]
- Hyperkalzämie[4]
- Hypomagnesiämie: Kann als Ko-Faktor das Auftreten eines PHT begünstigen (z. B. Torsades de pointes), ist aber nie alleinige Ursache eines Kammerflimmerns.
- Azidose, z. B. bei Niereninsuffizienz oder respiratorischer Insuffizienz (unzureichender Atemfunktion)
- Hypoxie
- Akute und subakute Ischämie (Durchblutungsstörungen), am häufigsten beim Herzinfarkt und bis 48 Stunden nach Beginn des Schmerzereignisses
- Reperfusion (Einschwemmung von Stoffwechselprodukten nach wiederhergestellter Durchblutung)
- Antiarrhythmika und Drogen:
- Ein verlängertes QTc-Intervall im Ruhe-EKG und ein langsamer Grundrhythmus sind Hinweise auf eine medikamenteninduzierte Torsade de pointes.
- Drogen, wie z. B. Kokain, oder andere Kokainderivate können zu Gefäßspasmen mit nachfolgenden ischämiebedingten Herzrhythmusstörungen führen.
- Stress (erhöhter Sympathikotonus)
- Vagus-Reizung bzw. starke vagotone Reaktion:
- Schlaf
- Wasserlassen (auch bekannt bei der Miktions-Synkope)
- Erholung direkt nach Beendigung einer starken körperlichen Anstrengung
- Plötzlicher Stop einer übermäßigen plötzlichen Aktivität
Außergewöhnliche Auslöser
- Stromschlag
- Herzbeuteltamponade
- Äußere mechanische Verletzung ( Schuss oder Stich u.ä)
Arrhythmie-Mechanismen
- Kreisende Erregung (Reentry)
- vermehrte Automatie, z. B. im Übergangsgewebe zwischen Narbe und gesundem Herzmuskel beispielsweise nach Infarkt oder bei HCM
- getriggerte Aktivität
Behandlung
Der drohende plötzliche Herztod wird nach Möglichkeit durch manuelle Reanimations-Maßnahmen behandelt. Neben der Wiederherstellung eines Minimalkreislaufes durch Herzdruck-massage und Beatmung wird möglichst frühzeitig mit Hilfe eines Defibrillators z.B. WelchAllyn AED erfolgen.
Bei Vorliegen einer therapierbaren Rhythmusstörung (VT, KF) erfolgt die kontrollierte Cardioreversion.
Außerhalb des Krankenhaus kommt es häufig nicht zur Reanimation. Eine Reanimation ist auch nur in ca. 30 % der Fälle erfolgreich. Der Erfolg und die Wahrscheinlichkeit, das Krankenhaus gesund, d. h. ohne hypoxischen Hirnschaden zu verlassen, ist vom Herzrhythmus bei Auffinden des Patienten und von der Qualität der Erstversorgung (Laienreanimation) abhängig.
| vorgefundener Rhythmus | erfolgreiche Reanimation | Verlassen der Klinik |
| Asystolie | < 10 % | 0-2 % |
| Entkoppelung | ca. 20 % | 11 % |
| Kammerflimmern | > 25 % | 11 % |
| Kammertachykardie | > 75 % | 65-70 % |
| nichtkardiale Ursachen | 40 % | 11 % |
Prävention
Es wird zwischen einer primären Prävention ohne Bestehen einer schwerwiegenden Rhythmusstörung und einer sekundären Prävention nach überlebtem Herzstillstand unterschieden.
Primäre Prävention
Die meisten Studien zur Primärprävention des PHT sind mit Postinfarktpatienten und mit Patienten mit einer strukturellen Herzerkrankung wie DCM und KHK durchgeführt worden. Eine Primärprävention ist durch eine optimale Therapie der zugrundeliegenden Herzerkrankung möglich. Dies umfasst bei KHK eine konsequente Therapie der Risikofaktoren und revaskularisierende (die Durchblutung wiederherstellende) Maßnahmen wie Koronarangioplastie und Bypassoperation. Nach einem Schlafapnoesyndrom sollte gesucht werden und, wenn es vorhanden ist, therapiert werden.
Medikamente
Für Patienten mit schwer eingeschränkter Pumpfunktion (Auswurffraktion < 35 %) gilt:
- Der Erfolg einer medikamentösen Primärprävention mit Amiodaron gilt als nicht gesichert. Die großen Primärpräventionsstudien zeigen einen günstigen Effekt auf die Inzidenz (Häufigkeit des Auftretens) des PHT bei Postinfarktpatienten, ohne die Gesamtsterblichkeit nennenswert zu beeinflussen.
- Betablocker reduzieren die Rate des plötzlichen Herztodes nach Myokardinfarkt um bis zu 30 % (MERIT-HF-Studie).
- Aldosteronantagonisten (Spironolacton, Eplerenon) zeigen eine 15%ige Senkung des PHT nach Herzinfarkt (EPHESUS-Studie).
- Angiotensin-Converting-Enzym-Hemmer (ACEH) vermindern nach den Ergebnissen einer Metaanalyse das Risiko eines PHT nach Infarkt um 20 %.
- Die primärpräventive Wirkung anderer Antiarrhythmika gilt als nicht gesichert hinsichtlich der Gesamtsterblichkeit, für Sotalol ist ein Anstieg der Sterblichkeit bei Postinfarktpatienten gesichert (SWORD-Studie).
Implantierbarer Kardioverter-Defibrillator (ICD)
Die Implantation eines ICD gilt nur bei folgenden Krankheitsbildern in ihrer primärpräventiven Wirkung als gesichert (MADIT-I-Studie)[5]:
- kurzdauernde (<30 sek.) ventrikuläre Tachykardie
- eingeschränkte Pumpfunktion
- künstlich auslösbares Kammerflimmern oder Kammertachykardie, überlebter Infarkt oder KHK, wobei keine Unterdrückung der Herzrhythmusstörungen durch Klasse-I-Antiarrhythmika möglich ist
oder
- schwer eingeschränkte Pumpfunktion (Auswurffraktion < 30 %) mindestens 1 Monat nach Herzinfarkt oder 3 Monate nach Bypassoperation (MADIT-II-Studie)[6].
Sekundäre Prävention des plötzlichen Herztodes (nach überlebtem plötzlichen Herzstillstand)
Überlebende des plötzlichen Herzstillstandes weisen innerhalb des ersten Jahres ein Rezidivrisiko ( Wiederhohlrisiko) von bis zu 30 % auf, vorausgesetzt, das Ereignis fand nicht im Rahmen eines akuten Herzinfarktes statt. Nach zwei Jahren steigt das Risiko bereits auf bis zu 45 % an.
Medikamente
Eine medikamentöse Sekundärprävention mit Antiarrhythmika ist einer ICD-Implantation deutlich unterlegen.
- Trotz einer akuten und chronischen Unterdrückung von Kammertachykardien und Kammerflimmern durch Klasse-I-Antiarrhythmika und Sotalol beträgt das Rezidivrisiko innerhalb der ersten zwei Jahre nach Ereignis 30-40 %.
- Amiodaron ist den Klasse-I-Antiarrhythmika zwar überlegen, dennoch bleibt eine Rezidivrate nach zwei Jahren von 18 %.
Implantierbarer Kardioverter-Defibrillator (ICD)
Ein ICD ist nach überlebtem plötzlichen Herzstillstand bei Kammerflimmern oder Kammertachykardie ohne Nachweis einer reversiblen Ursache zur Sekundärprävention absolut indiziert.
- Eine Metaanalyse belegt eine 27%ige Reduktion der Gesamtmortalität innerhalb von sechs Jahren nach Ereignis (AVID-, CASH- und CIDS-Studie)
- nur Patienten mit einer eingeschränkten Pumpfunktion (Auswurffraktion < 40 %) profitieren signifikant von einer ICD-Implantation gegenüber einer Amiodaron-Medikation. Bei Patienten mit einer gering oder gar nicht eingeschränkten Pumpfunktion (Auswurffraktion > 40 %) ist die ICD-Therapie einer Amiodaron-Therapie nicht überlegen (AVID-Subgruppenanalyse). Trotzdem wird zur Zeit eine Amidarontherapie nur als Begleittherapie zum ICD bei einem reanimierten Patienten empfohlen, um die Häufigkeit von Schockabgaben zu minimieren, oder für Patienten, die einen ICD ablehnen bzw. aus anderen Gründen nicht erhalten können.
Plötzlicher Tod aus nichtkardialer Ursache
Eine Reihe von nicht-kardialen Ursachen können ebenfalls einen plötzlichen Tod verursachen. So können etwa eine Lungenembolie, eine akute innere Blutung oder eine akute Vergiftung ebenfalls zu einem plötzlichen Tode führen.
Literaturhinweis
- Mewis, Riessen, Spyridopoulos (Hrsg.): Kardiologie compact - Alles für Station und Facharztprüfung. 2 Auflage. Thieme, Stuttgart, New York 2006, ISBN 3-13-130742-0, S. 629-649.
- Corrado D et al.: Does sports activity enhance the risk of sudden death in adolescents and young adults? J Am Coll Cardiol (2003) 42(11):1959-63. PMID 14662259
- Dichtl W et al: An uncommon coronary artery fistula causing survived sudden cardiac death in a young woman. Int J Cardiovasc Imaging (2005) 21(4):387-390. PMID 16047119
- Wilfried Kindermann, Axel Urhausen: Plötzlicher Herztod beim Sport. Bundesinstitut für Sportwissenschaft, Köln 2000, ISBN 3-89001-131-4, S. 1-55 (Fulltext im Web (pdf)).
- Mills AT et al.: Brugada syndrome: syncope in the younger patient and the risk of sudden cardiac death. Emerg Med J (2005) 22(8):604-6. PMID 16046779
- Priori SG et al.: Task Force on Sudden Cardiac Death of the European Society of Cardiology. Eur Heart J. 2001 Aug;22(16):1374-450. PMID 11482917
- Tabib A et al.: Circumstances of death and gross and microscopic observations in a series of 200 cases of sudden death associated with arrhythmogenic right ventricular cardiomyopathy and/or dysplasia. Circulation (2003) 108(24):3000-5. PMID 14662701